|
||||||||
|
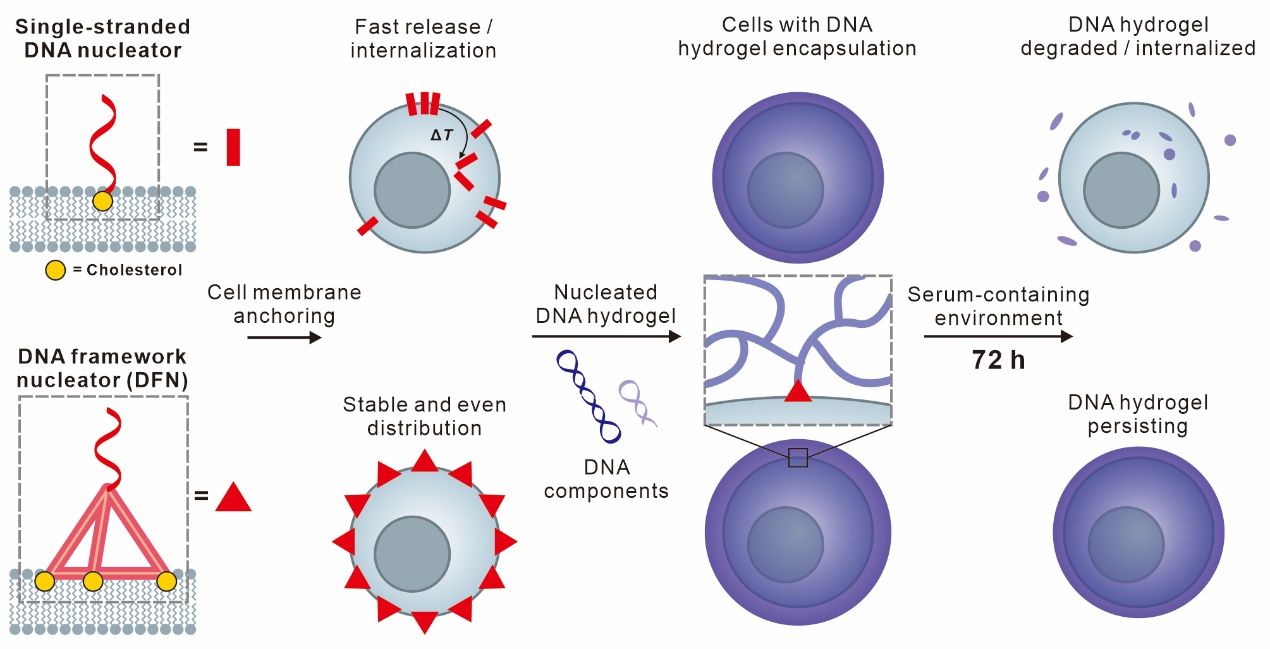
用仿生材料进行单细胞包裹在体外细胞培养与工程化调控中有巨大的应用价值。DNA水凝胶具有高度可编程的结构和机械特性,以及良好的生物相容性与可降解性,因此在细胞特异性捕获和检测、免疫疗法、细胞培养和命运调控以及体内组织修复方面已经显示出应用潜力。然而,在单细胞包裹中实现均匀性、稳定性和细胞相容性之间的平衡仍然是一个重大挑战。目前的单细胞包裹方法往往无法同时实现均匀、稳定且细胞友好的细胞封装。一方面,DNA单链作为成核剂在细胞表面上的稳定性较差,极大地影响了凝胶的生长密度、均匀性和稳定性。另一方面,引入聚合物或无机材料来改善这一问题,则会影响DNA水凝胶的可编程性和细胞相容性。 自然界中的多种细菌可以利用其外膜上稳定锚定的蛋白作为成核位点来介导纤维结构的高效聚合,从而产生稳定而致密的细菌被膜。这一机制可为哺乳动物的单细胞包裹提供启发。近日,上海大学的诸颖研究员和上海交通大学的樊春海教授,效仿细菌被膜的成核生长机制,利用DNA框架结构作为成核器(DFN)稳定锚定于细胞膜上,启动DNA水凝胶在单细胞表面的生长,构建了长时稳定且能抵御机械刺激的细胞保护层。
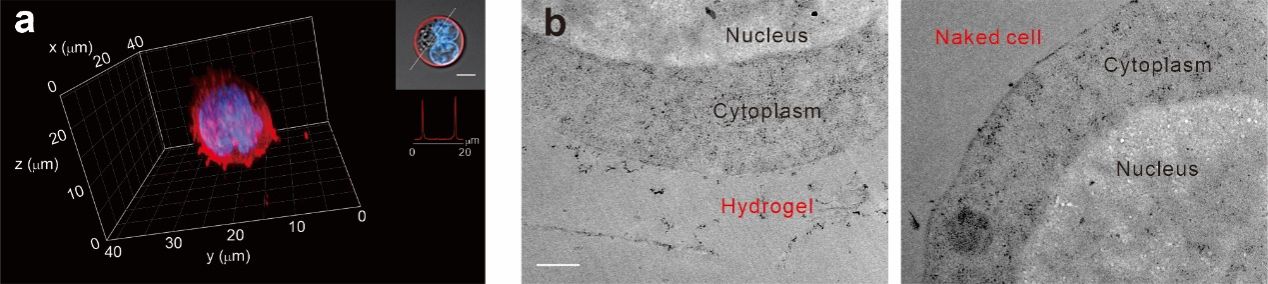
作者设计选择了三种不同的DNA框架成核器(DNA framework nucleators,DFN),分别是Y形成核器 Y-shaped(yDFN)、X形成核器X-shaped(xDFN)和四面体成核器tetrahedral DFN(tDFN),并以胆固醇修饰的单链DNA nucleotor作为对照。该结构包括三个模块:用于锚定细胞膜的疏水基团、用于引发HCR凝胶生长反应的引发链,以及用于组织前两者空间排布的DNA框架结构。 在测试的结构中,四面体形状的DFN可以均匀而稳定地存在于细胞膜上,有效地启动杂交链反应,从而为不同细胞系产生均匀密集但灵活的单细胞封装。
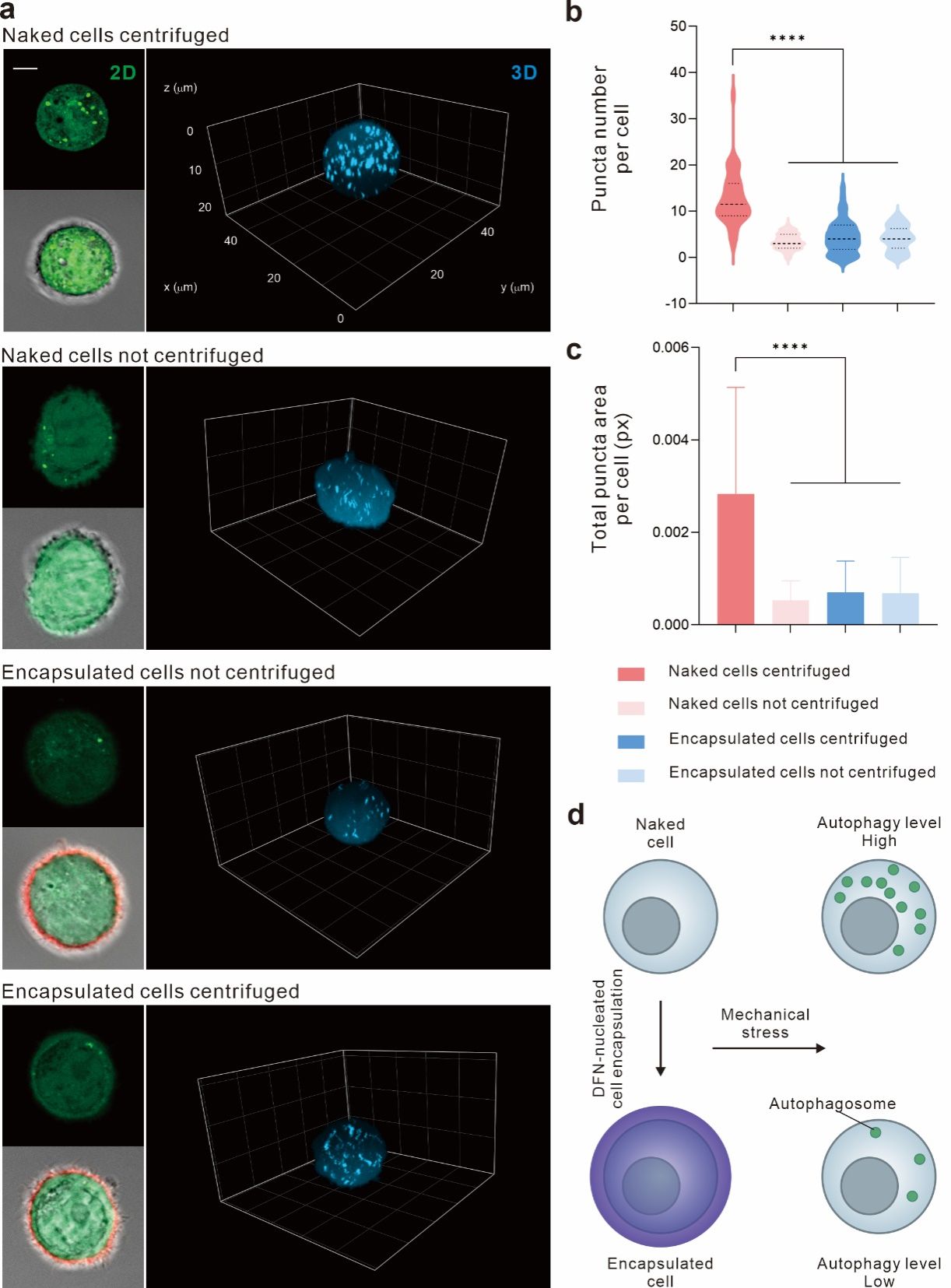
与裸细胞相比,受到机械应力刺激后的被包裹细胞显示出较低的自噬水平,表明DNA凝胶包裹能给细胞提供保护。这种方法为体外细胞工程应用提供了一种新工具。 本研究得到了国家重点研发计划、国家自然科学基金、2022年上海市“科技创新行动计划”基础研究项目和新基石科学基金的支持。 论文链接:https://doi.org/10.1002/anie.202319907 |
上一条:理学院材料生物学研究所诸颖研究员、王丽华研究员及合作团队在《Journal of the American Chemical Society》上发表最新研究成果
下一条:理学院材料生物学研究所孙乐乐与苏州大学团队合作在《Angewandte Chemie International Edition》发表最新研究成果